11月19日盤后,百利天恒發(fā)布公告,宣布與中國銀行四川分行達成戰(zhàn)略合作協(xié)議。根據(jù)協(xié)議,中國銀行四川分行將為百利天恒提供總額不低于80億元人民幣的綜合授信支持,以助力其戰(zhàn)略發(fā)展。這一消息引發(fā)市場廣泛關(guān)注,尤其是在公司近期一系列資本運作的背景下。
自2023年12月與跨國藥企百時美施貴寶(BMS)達成總價84億美元的合作以來,百利天恒便成為行業(yè)焦點。這筆交易創(chuàng)下全球抗體偶聯(lián)藥物(ADC)領域單個資產(chǎn)總交易金額的最高紀錄。隨后,公司于2024年1月在科創(chuàng)板上市,進一步擴大了其資本版圖。然而,公司的國際化進程并非一帆風順。今年初,百利天恒曾兩次向港交所提交招股書,但均因市場環(huán)境不佳而暫緩。公司創(chuàng)始人朱義表示,當時港股市場流動性不足,國際形勢動蕩,因此決定先回A股市場。
盡管如此,百利天恒并未放棄港股上市計劃。今年9月,公司完成39億元人民幣的定增,并第三次更新港股招股書。朱義曾向媒體透露,港股上市是公司國際化戰(zhàn)略的關(guān)鍵一步。然而,從其資本運作和研發(fā)投入來看,百利天恒似乎始終面臨資金壓力。
百利天恒與BMS的合作涉及核心產(chǎn)品iza-bren的共同開發(fā)。作為全球首創(chuàng)且唯一進入III期臨床階段的EGFR/HER3雙抗ADC,iza-bren的研發(fā)需要巨額資金支持。根據(jù)協(xié)議,雙方將共同分擔全球開發(fā)費用。百利天恒還計劃在未來五年內(nèi)成為一家在腫瘤領域領先的跨國藥企。為實現(xiàn)這一目標,公司不僅需要強大的藥物開發(fā)平臺和潛在重磅藥物,還需提升美國臨床開發(fā)能力,并建立全球商業(yè)化團隊。這些計劃無一不需要大量資金投入。
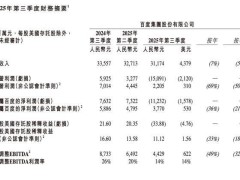
根據(jù)百利天恒2025年中報,公司目前有15款創(chuàng)新藥處于臨床試驗階段,其中3款已進入III期注冊臨床。iza-bren是其中的重點產(chǎn)品,共開展40余項臨床研究,包括3項全球關(guān)鍵注冊臨床和11項中國III期臨床,覆蓋多種腫瘤類型。如此龐大的研發(fā)管線意味著巨大的資金消耗。數(shù)據(jù)顯示,2023年以來,百利天恒的研發(fā)費用幾乎每年翻倍,今年前三季度已達17.72億元。截至第三季度末,公司現(xiàn)金及等價物余額為55.46億元,但仍難以覆蓋長期研發(fā)需求。
一位創(chuàng)新藥領域資深投資人表示,類似百利天恒這樣規(guī)模和發(fā)展階段的公司,擁有如此多的研發(fā)管線并不罕見,但其整體風格偏激進,資金壓力較大。當被問及公司同時開發(fā)眾多管線的原因時,朱義回應稱,公司的思路是“數(shù)據(jù)驅(qū)動、臨床需求驅(qū)動,再根據(jù)需求籌措資金”。
盡管面臨資金挑戰(zhàn),iza-bren的全球開發(fā)已取得重要進展。今年10月,百利天恒公告稱,iza-bren的全球II/III期關(guān)鍵注冊臨床試驗IZABRIGHT-Breast01已達成里程碑事件,觸發(fā)與BMS合作協(xié)議項下第一筆2.5億美元的近期或有付款條件。公司全資子公司SystImmune將于近期收到這筆款項。這意味著iza-bren不僅在首付款環(huán)節(jié),還在后續(xù)開發(fā)階段開始兌現(xiàn)商業(yè)價值。
國產(chǎn)創(chuàng)新藥出海后被海外藥企實質(zhì)性推進的案例并不少見。今年11月,輝瑞和百歐恩泰(BioNTech)先后公布了對PD-1雙抗的開發(fā)計劃。輝瑞的PD-1/VEGF雙抗PF-08634404將展開7項臨床研究,包括2項針對非小細胞肺癌和結(jié)直腸癌的全球III期研究。百歐恩泰從普米斯生物引進的PD-(L)1/VEGF雙抗Pumitamig也在推進針對小細胞肺癌、非小細胞肺癌和三陰乳腺癌的全球III期臨床。這些產(chǎn)品的定位均為下一代腫瘤基石性療法,旨在覆蓋多種腫瘤適應證,并探索與其他療法聯(lián)用的可能性。
海外藥企對中國創(chuàng)新藥資產(chǎn)的重視日益提升。前述投資人透露,全球前十的跨國藥企中,幾乎每月都有1-2位全球副總裁來中國參與項目合作或談判,主流藥企CEO也基本每年訪華一次。這一現(xiàn)象在前幾年極為罕見。銳正基因創(chuàng)始人王永忠也表示,跨國藥企正在擴大在中國的商務拓展團隊規(guī)模,細分程度也在提高。
摩根士丹利的研究預測,到2040年,中國藥物將占美國食藥監(jiān)局(FDA)批準數(shù)量的35%,而目前這一比例僅為5%。然而,國產(chǎn)創(chuàng)新藥要真正實現(xiàn)治病救人和商業(yè)回報的最大化,仍需完成全球臨床開發(fā)、注冊申報和商業(yè)化銷售的全流程。復宏漢霖首席商務發(fā)展官曹平曾指出,目前藥企間的合作多集中在早期資產(chǎn),但創(chuàng)新藥領域的不確定性較高,產(chǎn)品能否進入臨床、獲批上市或成為百億美元銷售額的重磅藥物仍是未知數(shù)。只有當中國公司原研開發(fā)的創(chuàng)新藥躋身全球“重磅炸彈”行列,中國創(chuàng)新藥才能真正迎來輝煌時代。